एनसीईआरटी समाधान कक्षा 11 रसायन अध्याय 7 अपचयोपचय अभिक्रियाएँ
एनसीईआरटी समाधान कक्षा 11 रसायन अध्याय 7 अपचयोपचय अभिक्रियाएँ के सवाल जवाब अभ्यास के प्रश्न उत्तर हिंदी और अंग्रेजी मीडियम में शैक्षणिक सत्र 2025-26 के अनुसार संशोधित रूप में यहाँ दिए गए हैं। कक्षा 11 रसायन शास्त्र पाठ 7 के समाधान सीबीएसई के साथ-साथ राजकीय बोर्ड के छात्रों के लिए भी उपयोगी हैं।
कक्षा 11 रसायन अध्याय 7 के लिए एनसीईआरटी समाधान
कक्षा 11 रसायन अध्याय 7 अपचयोपचय अभिक्रियाएँ के प्रश्न उत्तर
अपचयोपचय अभिक्रियाएँ
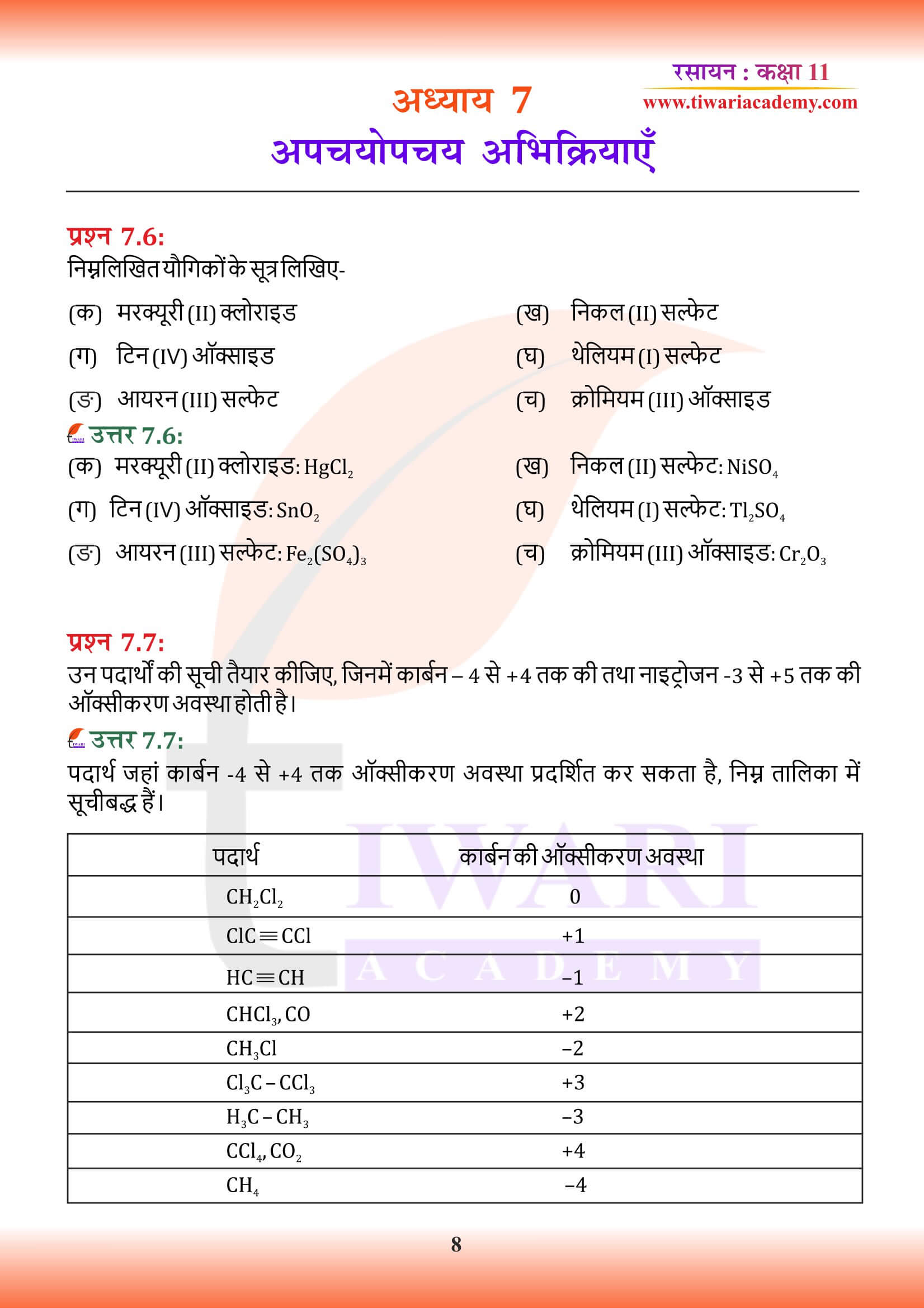
निम्नलिखित यौगिकों के सूत्र लिखिए-
(क) मरक्यूरी (II) क्लोराइड (ख) निकल (II) सल्फेट
(ग) टिन (IV) ऑक्साइड (घ) थेलियम (I) सल्फेट
(ङ) आयरन (III) सल्फेट (च) क्रोमियम (III) ऑक्साइड
उत्तर:
(क) मरक्यूरी (II) क्लोराइड: HgCl₂ (ख) निकल (II) सल्फेट: NiSO₄
(ग) टिन (IV) ऑक्साइड: SnO₂ (घ) थेलियम (I) सल्फेट: Tl₂SO₄
(ङ) आयरन (III) सल्फेट: Fe₂(SO₄)₃ (च) क्रोमियम (III) ऑक्साइड: Cr₂O₃
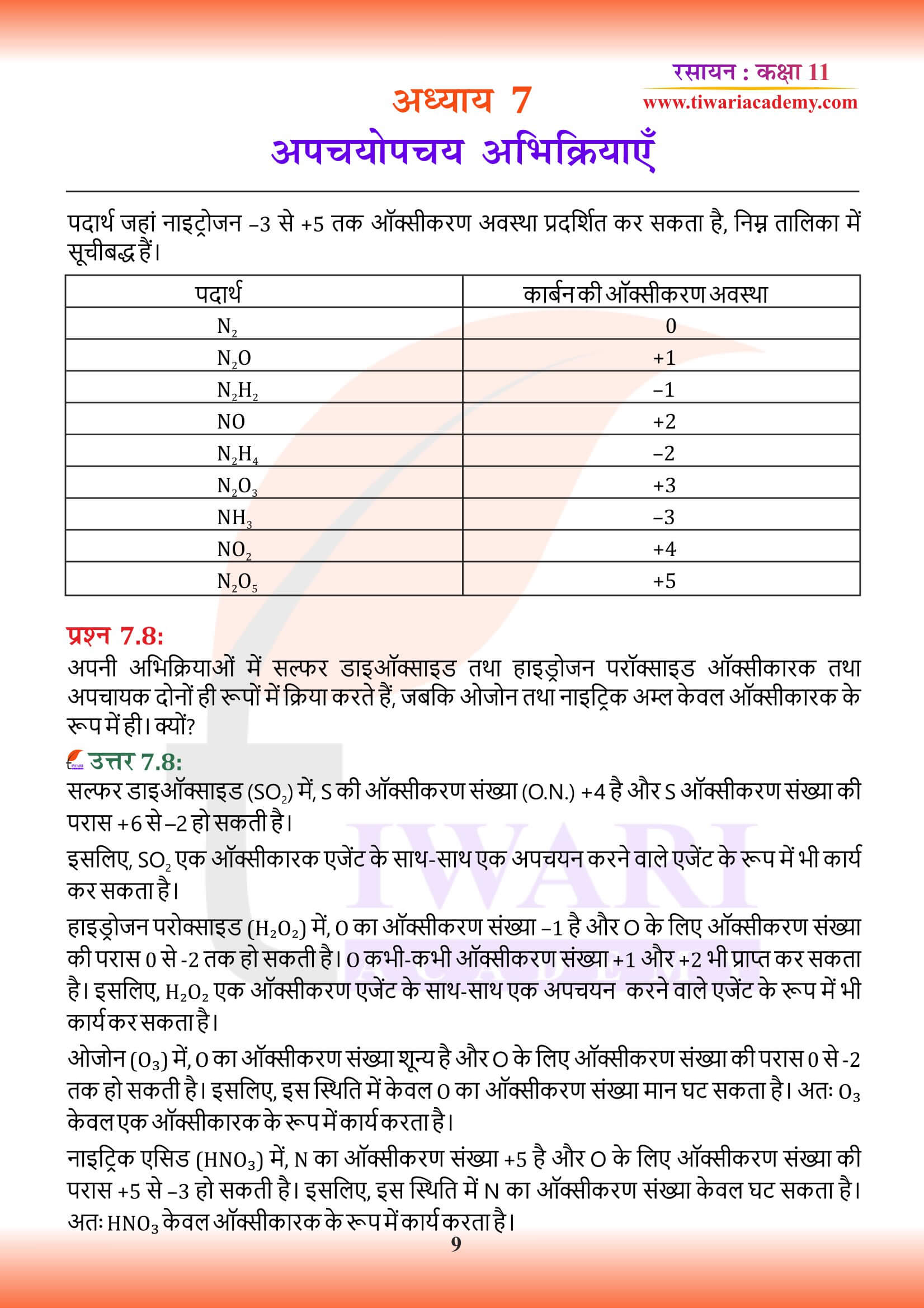
अपनी अभिक्रियाओं में सल्फर डाइऑक्साइड तथा हाइड्रोजन परॉक्साइड ऑक्सीकारक तथा अपचायक दोनों ही रूपों में क्रिया करते हैं, जबकि ओजोन तथा नाइट्रिक अम्ल केवल ऑक्सीकारक के रूप में ही। क्यों?
सल्फर डाइऑक्साइड (SO₂) में, S की ऑक्सीकरण संख्या (O.N.) +4 है और S ऑक्सीकरण संख्या की परास +6 से –2 हो सकती है।
इसलिए, SO₂ एक ऑक्सीकारक एजेंट के साथ-साथ एक अपचयन करने वाले एजेंट के रूप में भी कार्य कर सकता है।
हाइड्रोजन परोक्साइड (H₂O₂) में, O का ऑक्सीकरण संख्या –1 है और O के लिए ऑक्सीकरण संख्या की परास 0 से -2 तक हो सकती है। O कभी-कभी ऑक्सीकरण संख्या +1 और +2 भी प्राप्त कर सकता है। इसलिए, H₂O₂ एक ऑक्सीकरण एजेंट के साथ-साथ एक अपचयन करने वाले एजेंट के रूप में भी कार्य कर सकता है।
ओजोन (O₃) में, O का ऑक्सीकरण संख्या शून्य है और O के लिए ऑक्सीकरण संख्या की परास 0 से -2 तक हो सकती है। इसलिए, इस स्थिति में केवल O का ऑक्सीकरण संख्या मान घट सकता है। अतः O₃ केवल एक ऑक्सीकारक के रूप में कार्य करता है।
नाइट्रिक एसिड (HNO₃) में, N का ऑक्सीकरण संख्या +5 है और O के लिए ऑक्सीकरण संख्या की परास +5 से –3 हो सकती है। इसलिए, इस स्थिति में N का ऑक्सीकरण संख्या केवल घट सकता है। अतः HNO₃ केवल ऑक्सीकारक के रूप में कार्य करता है।
AgF₂एक अस्थिर यौगिक है। यदि यह बन जाए, तो यह यौगिक एक अति शक्तिशाली ऑक्सीकारक की भाँति कार्य करता है। क्यों?
AgF₂ में Ag की ऑक्सीकरण अवस्था +2 है। लेकिन, +2 ऑक्सीकरण अवस्था Ag की अस्थिर अवस्था है। इसलिए, जब भी AgF₂ बनता है, तो चांदी Ag⁺ बनाने के लिए एक इलेक्ट्रॉन को आसानी से स्वीकार कर लेती है। यह Ag के ऑक्सीकरण अवस्था को +2 से नीचे +1 की अधिक स्थिर अवस्था में लाने में मदद करता है। अतः, AgF₂ एक बहुत मजबूत ऑक्सीकारक के रूप में कार्य करता है।
प्रश्न:
Cs, Ne, I तथा F में ऐसे तत्त्व की पहचान कीजिए, जो
(क) केवल ऋणात्मक ऑक्सीकरण अवस्था प्रदर्शित करता है।
(ख) केवल धनात्मक ऑक्सीकरण अवस्था प्रदर्शित करता है।
(ग) ऋणात्मक तथा धनात्मक दोनों ऑक्सीकरण अवस्था प्रदर्शित करता है।
(घ) न ऋणात्मक और न ही धनात्मक ऑक्सीकरण अवस्था प्रदर्शित करता है।
उत्तर:
(क) F केवल -1 की ऋणात्मक ऑक्सीकरण अवस्था प्रदर्शित करता है।
(ख) Cs +1 के धनात्मक ऑक्सीकरण अवस्था को प्रदर्शित करता है।
(ग) I धनात्मक और ऋणात्मक दोनों ऑक्सीकरण अवस्थाओं को प्रदर्शित करता है। यह – 1, + 1, + 3, + 5, और + 7 की ऑक्सीकरण अवस्था प्रदर्शित करता है।
(घ) Ne की ऑक्सीकरण अवस्था शून्य है। यह न तो ऋणात्मक और न ही धनात्मक ऑक्सीकरण अवस्था प्रदर्शित करता है।
इस पुस्तक में दी गई आवर्त सारणी की सहायता से निम्नलिखित प्रश्नों के उत्तर दीजिए?
(क) संभावित अधातुओं के नाम बताइए, जो असमानुपातन की अभिक्रिया प्रदर्शित कर सकती हों।
(ख) किन्हीं तीन धातुओं के नाम बताइए, जो असमानुपातन अभिक्रिया प्रदर्शित कर सकती हों।
उत्तर:
असमानुपातन अभिक्रियाओं में, अभिक्रियाशील पदार्थों में से एक में हमेशा एक तत्व होता है जो कम से कम तीन ऑक्सीकरण अवस्थाओं में मौजूद हो सकता है।
(क) P, Cl, और S असमानुपातन अभिक्रियाएं दिखा सकते हैं क्योंकि ये तत्व तीन या अधिक ऑक्सीकरण अवस्थाओं में मौजूद हो सकते हैं।
(ख) Mn, Cu और Ga असमानुपातन अभिक्रिया दिखा सकते हैं क्योंकि ये तत्व तीन या अधिक ऑक्सीकरण अवस्थाओं में मौजूद हो सकते हैं।