एनसीईआरटी समाधान कक्षा 12 रसायन अध्याय 4 d एवं f ब्लॉक के तत्व
एनसीईआरटी समाधान कक्षा 12 रसायन विज्ञान अध्याय 4 d- एवं f- ब्लॉक के तत्व अभ्यास के प्रश्न उत्तर तथा पाठ्यनिहित प्रश्नों के हल सीबीएसई सत्र 2025-26 के लिए यहाँ से निशुल्क प्राप्त किए जा सकते हैं। कक्षा 12 रसायन शास्त्र के पाठ 4 के सभी प्रश्नों को यहाँ सरल तरीके से चरण दर चरण समझाया गया है।
एनसीईआरटी समाधान कक्षा 12 रसायन अध्याय 4
कक्षा 12 रसायन विज्ञान अध्याय 4 d एवं f ब्लॉक के तत्व के प्रश्न उत्तर
d एवं f ब्लॉक के तत्व
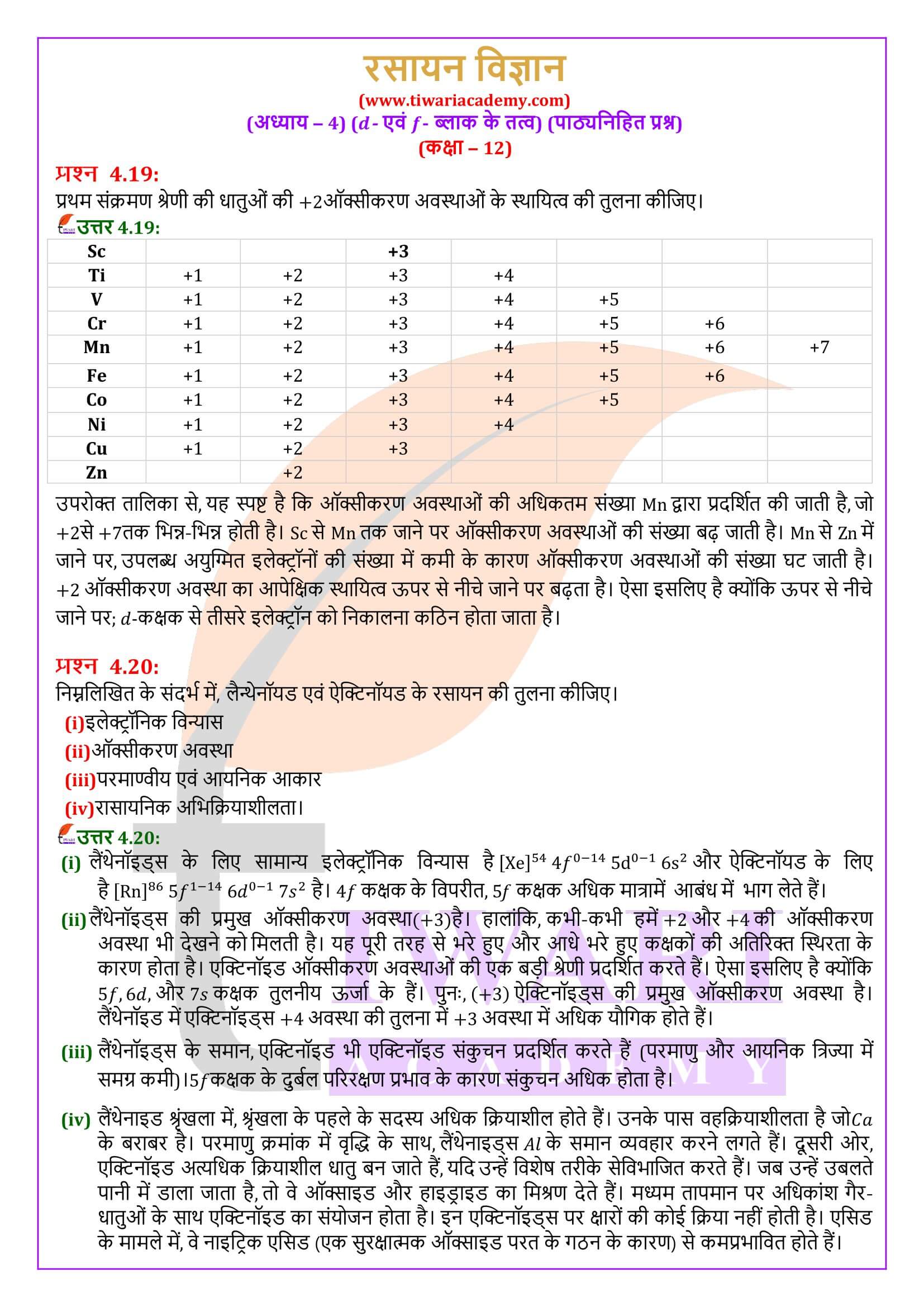
आवर्त सारणी के d- ब्लॉक में वर्ग 3 से 12 के तत्व आते हैं, जिसमें चारों दीर्घ आवर्तों में d कक्षक भरे जाते हैं। f- ब्लॉक के तत्व वे हैं जिनमें दीर्घ आवर्तों में 4f तथा 5f कक्षक उत्तरोत्तर भरे जाते हैं इन्हें आवर्त सारणी के नीचे एक अलग खण्ड में रखा गया है। d- एवं f-ब्लॉक के तत्वों को क्रमशः संक्रमण तत्व एवं आंतरिक संक्रमण तत्व भी कहते हैं।
संक्रमण तत्वों की श्रेणी
संक्रमण तत्वों की मुख्य रूप से चार श्रेणियाँ हैं, 3d श्रेणी (Sc से Zn), 4d श्रेणी (Y से Cd), तथा 5d श्रेणी (La तथा Hf से Hg) तथा चौथी 6d श्रेणी जिसमें Ac तथा Rf से Cn तक तत्व आते हैं। आंतरिक संक्रमण तत्वों की दो श्रेणियाँ, 4f (Cu से Le) तथा 5f (Th से Lr) क्रमशः लैन्थेनॉयड तथा ऐक्टिनॉयड कहलाती हैं।
कक्षा 12 रसायन विज्ञान अध्याय 4 बहुविकल्पीय प्रश्न उत्तर
एक संक्रमण तत्व X का +3 ऑक्सीकरण अवस्था में इलेक्ट्रॉनिक विन्यास [Ar]3d⁵ है। इसका परमाणु-क्रमांक क्या है?
Cu (II) का इलेक्ट्रॉनिक विन्यास 3d⁹ है, जबकि Cu(I) का 3d¹⁰ होता है। निम्नलिखित में से कौन-सा सही है?
अयुगलित इलेक्ट्रॉनों की उपस्थिति के कारण संक्रमण तत्व सामान्यतः रंगीन लवण बनाते हैं। ठोस अवस्था में निम्नलिखित में से कौन-सा यौगिक रंगीन होगा?
तत्वों की चुम्बकीय प्रकृति अयुगलित इलेक्ट्रॉनों की उपस्थिति पर निर्भर करती है। उस संक्रमण तत्व के विन्यास की पहचान कीजिए जो उच्चतम चुम्बकीय आघूर्ण प्रदर्शित करता है?
आवर्त सारणी में स्थिति
आवर्त सारणी का बड़ा मध्य भाग d- ब्लॉक ने घेरा हुआ है, जिसके दोनों ओर s- तथा p- ब्लॉक स्थित हैं। इनके परमाणुओं में उपांतिम ऊर्जा स्तरों के d- कक्षकों में इलेक्ट्रॉन भरे जाते हैं तथा इस प्रकार संक्रमण धातुओं की चार पंक्तियाँ अर्थात् 3d, 4d, 5d तथा 6d प्राप्त होती हैं।
d- ब्लॉक तत्वों के इलेक्ट्रॉनिक विन्यास
सामान्य रूप से इन तत्वों के बाह्य कक्षकों का इलेक्ट्रॉनिक विन्यास (n-1)d¹⁻¹⁰ ns¹⁻² है। (n-1) आंतरिक d कक्षकों को इंगित करता है, जिनमें एक से दस तक इलेक्ट्रॉन हो सकते हैं तथा बाह्यतम ns कक्षक में एक अथवा दो इलेक्ट्रॉन हो सकते हैं। परंतु (n-1)d तथा ns कक्षकों की ऊर्जाओं में बहुत कम अंतर के कारण इस सामान्य नियम के अनेक अपवाद हैं। पुनश्चः अर्ध एवं पूर्ण भरित कक्षकों का स्थायित्व अपेक्षाकृत अधिक होता है। इसका परिणाम 3d श्रेणी के संक्रमण तत्वों, Cr तथा Cu के इलेक्ट्रॉनिक विन्यासों में प्रतिबिंबित होता है। उदाहरण के लिए Cr में 3d⁴4s² के स्थान पर 3d⁵4s¹ विन्यास है। 3d व 4s कक्षकों की ऊर्जाओं में अंतर इतना कम है कि वह 4s इलेक्ट्रॉन के 3d कक्षक
में प्रवेश को रोक नहीं पाता। इसी प्रकार से Cu में इलेक्ट्रॉनिक विन्यास 3d⁹4s² न होकर 3d¹⁰4s¹ है।
कक्षा 12 रसायन विज्ञान अध्याय 4 एमसीक्यू उत्तर
लैंथेनॉयडों के लिए निम्नलिखित में से कौन-सी ऑक्सीकरण अवस्था सभी में होती है?
जब KMnO₄ विलयन को ऑक्सैलिक अम्ल विलयन में मिलाया जाता है तो प्रारम्भ में इसका विरंजीकरण धीमा होता है, परन्तु कुछ समय बाद यह तात्क्षणिक हो जाता है, क्योंकि
ऐक्टिनॉयड श्रेणी में 14 तत्व हैं। निम्नलिखित में से कौन-सा तत्व इस श्रेणी का सदस्य नहीं है?
जब धातुओं के क्रिस्टल-जालकों के बीच छोटे परमाणु फंस जाते हैं, तो अंतराकाशी यौगिक बनते हैं। निम्नलिखित में से कौन-सा अंतराकाशी यौगिकों का अभिलक्षणिक गुण नहीं है?
आंतर संक्रमण तत्व (f-ब्लॉक)
f-ब्लॉक की दो श्रेणियाँ हैं, लैन्थेनॉयड (लैन्थेनम के बाद के चौदह तत्व) तथा ऐक्टिनॉयड (ऐक्टिनियम के बाद के चौदह तत्व)। चूँकि लैन्थेनम तथा लैन्थेनॉयड में सन्निकटता पाई जाती है अतः, लैन्थेनॉयडों की चर्चा में लैन्थेनम भी सम्मिलित रहता है। इन तत्वों के लिए सामान्य संकेत La प्रयुक्त होता है। इसी प्रकार से ऐक्टिनॉयड तत्वों की चर्चा में ऐक्टिनियम भी इस श्रेणी के चौदह तत्वों के साथ सम्मिलित रहता है।
कक्षा 12 रसायन विज्ञान अध्याय 4 के महत्वपूर्ण प्रश्न उत्तर
Cr की प्रथम आयनन एन्थैल्पी Zn की अपेक्षा कम क्यों है?
d⁵ के स्थायित्व के कारण Cr की आयनन एन्थैल्पी निम्न होती है और Zn के लिए मान उच्चतर होता है क्योंकि इसमें इलेक्ट्रॉन 4s कक्षक से निकलता है।
संक्रमण तत्व उच्च गलनांक प्रदर्शित करते हैं, क्यों?
संक्रमण धातुओं के उच्च गलनांक दे इलेक्ट्रॉन के अतिरिक्त बड़ी संख्या में (n-1)d इलेक्ट्रॉनों के अंतरापरमाणुक धात्विक बंधन में भाग लेने के कारण होते हैं।
संक्रमण तत्वों की दूसरी और तीसरी पंक्तियाँ, पहली पंक्ति की अपेक्षा, परस्पर अधिक समानता रखती हैं। समझाइए क्यों?
लैंथेनॉयड संकुचन के कारण, संक्रमण तत्वों की दूसरी और तीसरी पंक्ति की परमाणु त्रिज्याएँ लगभग बराबर हो जाती हैं। अतः उनमें पहली पंक्ति की अपेक्षा परस्पर अधिक समानता होती है।
लैन्थेनॉयड
संक्रमण श्रेणी की तुलना में लैन्थेनॉयड आपस में अधिक सन्निकट समानताएं प्रदर्शित करते हैं। इन तत्वों में केवल एक स्थायी ऑक्सीकरण अवस्था होती है तथा इनका रसायन इन समान गुणों वाले तत्वों के आकार तथा नाभिकीय आवेश में हुए अल्प परिवर्तन के श्रेणी में प्रभाव की समीक्षा करने का उत्तम अवसर प्रदान करता है।
इलेक्ट्रॉनिक विन्यास
यह देखा जा सकता है कि इन सभी परमाणुओं के इलेक्ट्रॉनिक विन्यास में 6s² एक समान है, परंतु 4f स्तर पर परिवर्तनशील निवेशन है। यद्यपि इन सभी तत्वों के त्रिधनात्मक इलेक्ट्रॉनिक विन्यास (लैन्थेनॉयडों की अति स्थायी ऑक्सीकरण अवस्था) का स्वरूप 4fⁿ है (बढ़ते हुए परमाणु क्रमांक के साथ n = 1 से 14 तक)।
कक्षा 12 रसायन शास्त्र अध्याय 4 के लिए एनसीईआरटी समाधान कहाँ से डाउनलोड करें?
कक्षा 12 के लिए रसायन विज्ञान के अध्याय 4 अभ्यास के प्रश्न उत्तर अधिकतर वेबसाइट पर पीडीएफ के रूप में मुफ्त डाउनलोड के लिए उपलब्ध है। सीबीएसई एनसीईआरटी समाधान का पीडीएफ तिवारी अकादमी वेबसाइट पर भी नए संस्करण में संशोधित रूप में दिया गया है। इसके माध्यम से छात्र कम समय में भी परीक्षा की तैयारी उचित ढंग से कर सकते हैं। कक्षा 12 रसायन शास्त्र के पाठ 4 के प्रश्न उत्तर यहाँ विस्तार से दिए गए हैं। ये सभी प्रश्न उत्तर तथा नोट्स विषय विशेषज्ञों द्वारा हल किए गए हैं ताकि छात्रों को उत्तम समाधान प्राप्त हो सके।
कक्षा 12 के छात्रों के लिए एनसीईआरटी रसायन विज्ञान पाठ 4 के समाधान क्यों उपयोगी हैं?
बारहवीं कक्षा में रसायन विज्ञान अध्याय 4 के अभ्यास तथा पाठ्यनिहित प्रश्नों के समाधान छात्रों को पाठ समझने में मदद करते हैं। यदि किसी प्रश्न के उत्तर में छात्रों को कोई दुविधा हो तो वे इन समाधानों की मदद से उसे आसानी से हल कर सकते हैं। कक्षा 12 रसायन के लिए एनसीईआरटी समाधान छात्रों को उन्नत शिक्षण प्रदान करने के उद्देश्य से बनाए गए हैं। प्रश्नों को हल करने के लिए रेखाचित्रों तथा पर्याप्त उदाहरणों का प्रयोग किया गया है। 12वीं कक्षा रसायन शास्त्र के ये सभी समाधान विशेषज्ञों द्वारा विकसित किया गया है जिसमें विस्तृत रूप में चरण-दर-चरण प्रश्न उत्तर की व्याख्या की गई है।
कक्षा 12 रसायन के पाठ 4 से d और f ब्लॉक के तत्वों को समझने के लिए एनसीईआरटी समाधान का प्रयोग कैसे करें?
12वीं कक्षा रसायन शास्त्र के अध्याय 4 को विस्तृत रूप से समझने के लिए एनसीईआरटी समाधान को एक सहायक के रूप में प्रयोग किया जा सकता है। यह सीबीएसई तथा राजकीय बोर्ड के छात्रों की बोर्ड परीक्षा के लिए बहुत मददगार होगी क्योंकि यह अभ्यास तथा पाठ्यनिहित प्रश्नों और उदाहरणों को आरेखों और दृष्टांतों के आधार पर विस्तृत रूप से समझता है। इन समाधानों की मदद से छात्रों के लगभग सभी संदेह समाप्त हो जाते हैं। इसमें आंतरिक संक्रमण धातुओं के इलेक्ट्रॉनिक विन्यास, ऑक्सीकरण और रासायनिक प्रतिक्रिया से संबंधित सभी महत्वपूर्ण विषयों को विस्तृत रूप में समझाया गया है। इसके द्वारा छात्र आवर्त सारणी में d और f ब्लॉक तत्वों की स्थिति को समझने में सक्षम होंगे।