एनसीईआरटी समाधान कक्षा 7 विज्ञान जिज्ञासा अध्याय 4 धातुओं और अधातुओं का संसार
कक्षा 7 की एनसीईआरटी विज्ञान पाठ्यपुस्तक जिज्ञासा का अध्याय 4 — धातुओं और अधातुओं का संसार — विद्यार्थियों को हमारे दैनिक जीवन में उपयोग होने वाली सामग्रियों की रोचक दुनिया से परिचित कराता है। इस अध्याय में यशवंत और आनंदी नामक दो बच्चे एक अनुभवी लोहार सुदर्शन चाचा से मिलते हैं और धातुओं के गुणों को प्रयोगों द्वारा समझते हैं। अध्याय में धातुओं के प्रमुख भौतिक गुण — जैसे आघातवर्धनीयता (हथौड़े से पीटकर चादर बनाना), तन्यता (तार में खींचना), ध्वानिकता (धनधनाहट की आवाज़), ऊष्मा एवं विद्युत चालकता — को सरल क्रियाकलापों के माध्यम से समझाया गया है। इसके साथ ही लोहे पर जंग लगने की प्रक्रिया, धातुओं पर वायु और जल के प्रभाव तथा अधातुओं (जैसे सल्फर, कोयला, ऑक्सीजन, नाइट्रोजन) के विशिष्ट गुणों पर भी विस्तार से चर्चा की गई है। यह अध्याय विद्यार्थियों को यह समझने में सहायता करता है कि धातुएँ और अधातुएँ हमारे जीवन, उद्योग और प्रकृति में किस प्रकार अत्यंत महत्त्वपूर्ण भूमिका निभाती हैं।
कक्षा 7 की एनसीईआरटी विज्ञान जिज्ञासा का अध्याय 4 के प्रश्न उत्तर
1. किस धातु का उपयोग खाद्य पदार्थों के संवेष्टन (पैकेजिंग) के लिए सामान्यतः किया जाता है क्योंकि यह धातु सस्ती होती है और इसकी पतली चादरों को सरलता से किसी भी आकार में मोड़ा जा सकता है?
(i) ऐलुमिनियम
(ii) ताँबा
(iii) लोहा
(iv) सोना
उत्तर:
(i) ऐलुमिनियम
ऐलुमिनियम एक सस्ती धातु है जो बहुत आघातवर्धनीय होती है यानी इसे पीटकर बहुत पतली चादरों में बदला जा सकता है। इसीलिए इसका उपयोग खाने की चीजों को लपेटने के लिए किया जाता है। ताँबा और सोना महँगी धातुएँ हैं और लोहा इतना लचीला नहीं होता।
2. निम्नलिखित में से कौन-सी धातु जल के संपर्क में आने पर आग पकड़ लेती है?
(i) ताँबा
(ii) ऐलुमिनियम
(iii) जिंक
(iv) सोडियम
उत्तर:
(iv) सोडियम
सोडियम एक बहुत क्रियाशील धातु है जो जल और ऑक्सीजन के साथ बहुत तेजी से अभिक्रिया करती है। इस अभिक्रिया में इतनी अधिक ऊष्मा उत्पन्न होती है कि आग लग जाती है। इसीलिए सोडियम को मिट्टी के तेल में रखकर संरक्षित किया जाता है ताकि यह नमी और वायु के संपर्क में न आए। ताँबा, ऐलुमिनियम और जिंक जल से ऐसी खतरनाक अभिक्रिया नहीं करते।
3. कारण सहित बताएँ कि निम्नलिखित कथन सत्य हैं अथवा असत्य।
(i) ऐलुमिनियम और ताँबा, पात्रों और मूर्तियों को बनाने के लिए उपयोग की जाने वाली अधातुओं के उदाहरण हैं।
(ii) धातुएँ ऑक्सीजन के साथ मिलकर ऑक्साइड बनाती हैं जिनका विलयन नीले लिटमस पत्र को लाल में परिवर्तित कर देता है।
(iii) ऑक्सीजन श्वसन के लिए एक आवश्यक अधातु है।
(iv) ताँबे के पात्रों का उपयोग जल उबालने के लिए किया जाता है क्योंकि वे विद्युत के सुचालक होते हैं।
उत्तर:
(i) असत्य
ऐलुमिनियम और ताँबा धातुएँ हैं, अधातु नहीं। धातुओं में द्युतिमयता, आघातवर्धनीयता, तन्यता और ऊष्मा की सुचालकता जैसे गुण होते हैं। इन्हीं गुणों के कारण इन धातुओं से पात्र और मूर्तियाँ बनाई जाती हैं।
(ii) असत्य
धातुओं के ऑक्साइड क्षारीय प्रकृति के होते हैं। क्षारीय पदार्थ लाल लिटमस पत्र को नीला करते हैं न कि नीले लिटमस पत्र को लाल। नीले लिटमस पत्र को लाल अम्लीय पदार्थ करते हैं। अधातुओं के ऑक्साइड अम्लीय होते हैं।
(iii) सत्य
ऑक्सीजन एक अधातु है जो हम सभी जीवों के श्वसन के लिए बिल्कुल जरूरी है। इसके बिना हम जीवित नहीं रह सकते। यह वायु में लगभग 21 प्रतिशत होती है।
(iv) असत्य
ताँबे के पात्रों का उपयोग जल उबालने के लिए इसलिए किया जाता है क्योंकि ताँबा ऊष्मा का सुचालक है न कि इसलिए कि यह विद्युत का सुचालक है। खाना पकाने में ऊष्मा का चालन काम आता है, विद्युत का चालन नहीं।
4. आभूषण बनाने के लिए केवल कुछ ही धातुएँ उपयुक्त क्यों हैं?
उत्तर:
आभूषण बनाने के लिए धातु में कुछ विशेष गुण होने जरूरी हैं। पहली बात यह कि धातु चमकदार यानी द्युतिमय होनी चाहिए ताकि आभूषण सुंदर दिखे। दूसरी बात यह कि धातु आघातवर्धनीय और तन्य होनी चाहिए ताकि उसे पतली चादरों और बारीक तारों के रूप में ढाला जा सके। तीसरी बात यह कि धातु को वायु और नमी से जल्दी नुकसान नहीं होना चाहिए यानी वह संक्षारण-प्रतिरोधी होनी चाहिए। सोना और चाँदी इन सभी गुणों को पूरा करती हैं इसलिए ये आभूषण बनाने के लिए उपयुक्त हैं। लोहा जंग लगने की वजह से और कोयला-सल्फर अधातु होने की वजह से अनुपयुक्त हैं।
5. स्तंभ I में दी गई धातुओं और अधातुओं के उपयोगों को स्तंभ II में दी गई धातुओं और अधातुओं के अव्यवस्थित नामों से सुमेलित कीजिए।
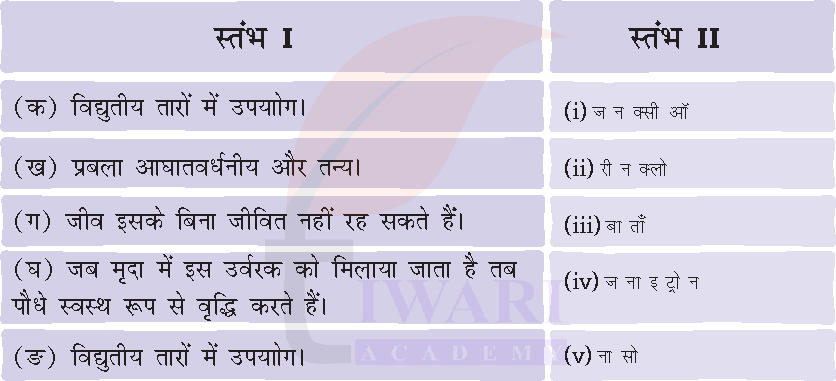
उत्तर:
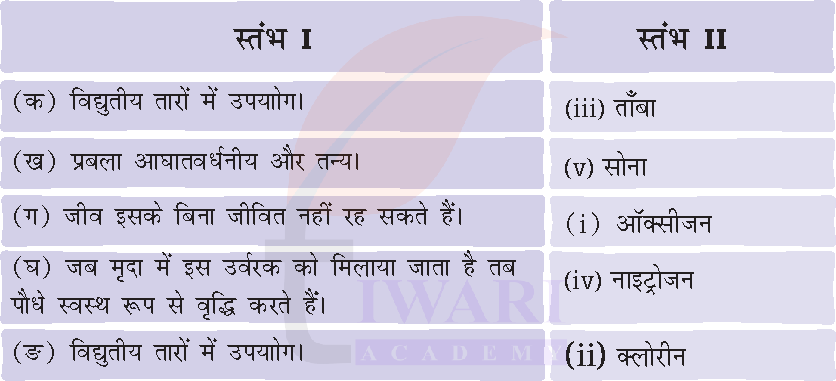
(क) विद्युतीय तारों में उपयोग → (iii) ताँबा
(ख) प्रबल आघातवर्धनीय और तन्य → (v) सोना
(ग) जीव इसके बिना जीवित नहीं रह सकते हैं → (i) ऑक्सीजन
(घ) जब मृदा में इस उर्वरक को मिलाया जाता है तब पौधे स्वस्थ रूप से वृद्धि करते हैं → (iv) नाइट्रोजन
(ङ) जल-शुद्धिकरण में इसका उपयोग किया जाता है → (ii) क्लोरीन
6. क्या होता है जब मैग्नीशियम और सल्फर, ऑक्सीजन के साथ अभिक्रिया करते हैं? निर्मित उत्पादों की प्रकृति में क्या प्रमुख अंतर होता है?
उत्तर:
जब मैग्नीशियम ऑक्सीजन के साथ अभिक्रिया करता है तो मैग्नीशियम ऑक्साइड बनता है। मैग्नीशियम एक धातु है इसलिए इसका ऑक्साइड क्षारीय प्रकृति का होता है। यह लाल लिटमस पत्र को नीला कर देता है।
जब सल्फर ऑक्सीजन के साथ अभिक्रिया करता है तो सल्फर डाइऑक्साइड गैस बनती है। सल्फर एक अधातु है इसलिए इसका ऑक्साइड अम्लीय प्रकृति का होता है। जल में घोलने पर यह सल्फ्यूरस अम्ल बनाता है और नीले लिटमस पत्र को लाल कर देता है।
निर्मित उत्पादों में प्रमुख अंतर यह है कि मैग्नीशियम ऑक्साइड क्षारीय है जबकि सल्फर डाइऑक्साइड का विलयन अम्लीय है।
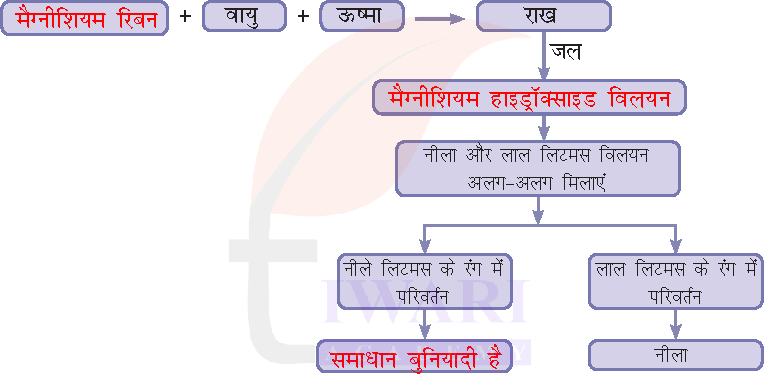
7. निम्नलिखित आरेख को पूरा कीजिए।
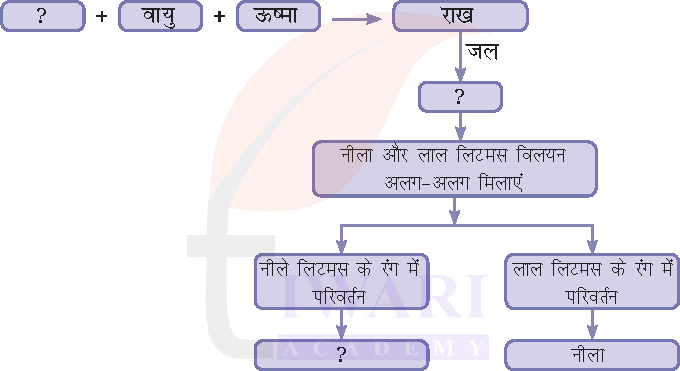
उत्तर:
1. मैग्नीशियम
2. मैग्नीशियम ऑक्साइड का विलयन
3. कोई परिवर्तन नहीं
8. आपको निम्नलिखित सामग्रियाँ दी गई हैं। उनमें से जल उबालने हेतु पात्र बनाने के लिए आप किस सामग्री का चयन सबसे उपयुक्त समझते हैं और क्यों? चर्चा कीजिए।
लोहा, ताँबा, सल्फर, कोयला, प्लास्टिक, लकड़ी, गत्ता
उत्तर:
ताँबा सबसे उपयुक्त सामग्री है।
ताँबे का चयन इसलिए सबसे उचित है क्योंकि ताँबा ऊष्मा का अच्छा सुचालक है जिससे गर्मी जल्दी और समान रूप से जल में पहुँचती है। यह धातु कठोर और मजबूत होती है। यह जल के साथ आसानी से अभिक्रिया नहीं करती। इसे किसी भी आकार में ढाला जा सकता है।
सल्फर, कोयला और गत्ता जल नहीं सकते इसलिए अनुपयुक्त हैं। प्लास्टिक और लकड़ी गर्म होने पर जल या पिघल जाते हैं इसलिए ये भी अनुपयुक्त हैं। लोहा ऊष्मा का चालक तो है लेकिन जंग लगने की समस्या रहती है।
9. आपको लोहे की तीन कीलें दी गई हैं जिनमें से प्रत्येक क्रमशः तेल, जल और सिरके में डूबी हुई हैं। कौन-सी लोहे की कील में जंग नहीं लगेगा और क्यों?
उत्तर:
तेल में डूबी लोहे की कील में जंग नहीं लगेगा।
हमने पढ़ा है कि लोहे में जंग लगने के लिए जल और वायु दोनों का एक साथ उपस्थित होना अनिवार्य है। तेल में डूबी कील वायु और नमी के संपर्क से पूरी तरह सुरक्षित रहती है इसलिए इसमें जंग नहीं लगेगा।
जल में डूबी कील में जल की उपस्थिति है और ऊपर से वायु भी उपलब्ध हो सकती है इसलिए उसमें जंग लग सकता है। सिरका अम्लीय है और यह लोहे की सतह को और तेजी से क्षतिग्रस्त कर सकता है।
10. धातुओं और अधातुओं के दैनिक जीवन में उपयोग को उनके विभिन्न गुणों के आधार पर कैसे निर्धारित किया जाता है?
उत्तर:
धातुओं और अधातुओं के उपयोग उनके गुणों पर निर्भर करते हैं।
- धातुएँ ऊष्मा और विद्युत की सुचालक होती हैं इसलिए खाना पकाने के बर्तन धातु से बनाए जाते हैं और विद्युत तारों में ताँबे का उपयोग किया जाता है।
- धातुएँ आघातवर्धनीय और तन्य होती हैं इसलिए उनसे चादरें और तार बनाए जाते हैं।
- धातुएँ द्युतिमय होती हैं इसलिए आभूषण बनाने में उनका उपयोग होता है।
- धातुएँ कठोर होती हैं इसलिए कृषि उपकरण और इमारतें बनाने में उपयोगी हैं।
अधातुओं में भी कई महत्वपूर्ण उपयोग हैं।
- ऑक्सीजन श्वसन के लिए जरूरी है।
- क्लोरीन जल शुद्धिकरण में काम आती है।
- नाइट्रोजन उर्वरकों में उपयोगी है।
- रबड़ और प्लास्टिक विद्युत कुचालक हैं इसलिए तारों के आवरण बनाने में काम आते हैं।
11. लोहे को जंग लगने से बचाने के उपायों में से एक है कि उस पर जिंक धातु की एक पतली परत चढ़ाना। चूँकि सल्फर जल के साथ अभिक्रिया नहीं करता है तो क्या इसका उपयोग इस उद्देश्य के लिए किया जा सकता है? अपने उत्तर की पुष्टि कीजिए।
उत्तर:
नहीं, सल्फर का उपयोग इस उद्देश्य के लिए नहीं किया जा सकता।
यह सच है कि सल्फर जल के साथ अभिक्रिया नहीं करता। लेकिन जिंक धातु की परत चढ़ाना सिर्फ इस कारण नहीं किया जाता। इसके लिए परत चढ़ाने वाले पदार्थ में कई जरूरी गुण होने चाहिए।
सल्फर एक अधातु है जो भंगुर होती है यानी यह आसानी से टूट जाती है। इसे लोहे की सतह पर मजबूती से चिपकाई जाने वाली सुरक्षात्मक परत के रूप में नहीं चढ़ाया जा सकता। इसके अलावा सल्फर वायु में ऑक्सीजन के साथ अभिक्रिया करके सल्फर डाइऑक्साइड बनाता है जो स्वयं हानिकारक है। जिंक धातु होने के कारण लोहे की सतह पर मजबूती से चिपकती है और एक टिकाऊ सुरक्षात्मक परत बनाती है।
12. एक लोहार उपकरण बनाने से पूर्व लोहे को गरम करता है। इस प्रक्रिया में गरम करना क्यों आवश्यक है?
उत्तर:
लोहार लोहे को भट्टी में गरम करता है क्योंकि गरम करने पर लोहा सुर्ख लाल हो जाता है और मुलायम पड़ जाता है। इस अवस्था में लोहे की आघातवर्धनीयता बढ़ जाती है यानी इसे आसानी से हथौड़े से पीटकर मनचाहा आकार दिया जा सकता है। ठंडे लोहे को इच्छित आकार देना बहुत कठिन होता है क्योंकि वह बहुत कठोर होता है। गरम करने के बाद लोहे को किसी भी आकार में ढालना आसान हो जाता है जैसे कुल्हाड़ी, फावड़ा, कीला आदि। जब तैयार उपकरण को ठंडा किया जाता है तो वह उसी आकार में कठोर हो जाता है।

